1. Temel bilgiler (deneysel kısmı görmek istiyorsanız, lütfen doğrudan ikinci kısma aktarın)
Konvansiyonel PCR'nin bir türev reaksiyonu olan Real time PCR, esasen PCR amplifikasyon reaksiyonunun her döngüsündeki amplifikasyon ürünü miktarındaki değişimi floresan sinyalinin değişimi aracılığıyla gerçek zamanlı olarak izler ve başlangıç şablonunu ct değeri ile standart eğri arasındaki ilişki aracılığıyla kantitatif olarak analiz eder.
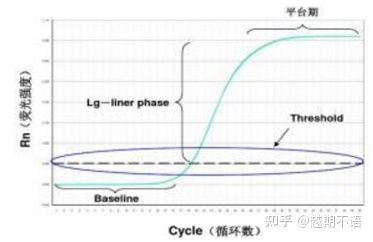
RT-PCR'nin spesifik verileri şunlardır:taban çizgisi, floresan eşiğiVeCt değeri.
| temel: | 3.-15. döngünün floresan değeri, ara sıra yapılan ölçüm hatasından kaynaklanan taban çizgisidir (taban çizgisi). |
| Eşik (eşik): | Amplifikasyon eğrisinin üstel büyüme bölgesinde uygun bir konuma ayarlanan flüoresan tespit limitini ifade eder, genellikle taban çizgisinin standart sapmasının 10 katıdır. |
| BT değeri: | Her reaksiyon tüpündeki floresans değeri eşiğe ulaştığında PCR döngülerinin sayısıdır. Ct değeri, ilk şablonun miktarı ile ters orantılıdır. |
RT-PCR için ortak etiketleme yöntemleri:
| yöntem | avantaj | eksiklik | uygulama kapsamı |
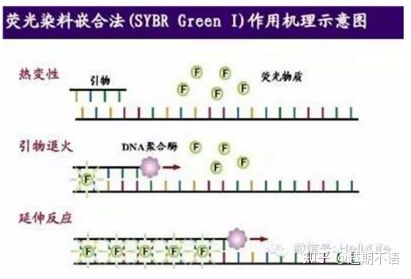
| SYBR YeşilⅠ | Geniş uygulanabilirlik, hassas, ucuz ve kullanışlı | Astar gereksinimleri yüksektir, spesifik olmayan bantlara eğilimlidir | Çeşitli hedef genlerin kantitatif analizi, gen ifadesi üzerine araştırma ve transgenik rekombinant hayvanlar ve bitkiler üzerinde araştırma için uygundur. |
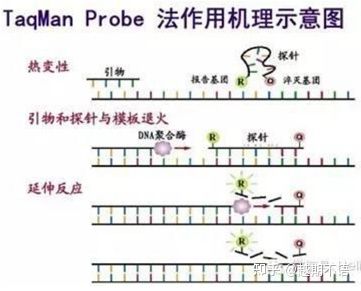
| taqman | İyi özgüllük ve yüksek tekrarlanabilirlik | Fiyat yüksektir ve yalnızca belirli hedefler için uygundur. | Patojen tespiti, ilaç direnci gen araştırması, ilaç etkinliği değerlendirmesi, genetik hastalıkların teşhisi. |
| moleküler işaret | Yüksek özgüllük, floresans, düşük arka plan | Fiyatı yüksektir, sadece belirli bir amaca uygundur, tasarımı zordur ve fiyatı yüksektir. | Spesifik gen analizi, SNP analizi |
2. Deneysel adımlar
2.1 Deneysel gruplama hakkında- Grupta birden fazla kuyu bulunmalı ve biyolojik tekrarlar olmalıdır.
| ① | Boş kontrol | Deneylerde hücre büyüme durumunu saptamak için kullanılır |
| ② | Negatif kontrol siRNA (spesifik olmayan siRNA dizisi) | RNAi eyleminin özgüllüğünü gösterin.siRNA, 200nM'lik bir konsantrasyonda spesifik olmayan stres tepkisini indükleyebilir. |
| ③ | Transfeksiyon Reaktif Kontrolü | Transfeksiyon reaktifinin hücrelere toksisitesini veya hedef genin ekspresyonu üzerindeki etkisini hariç tutun |
| ④ | hedef gene karşı siRNA | Hedef genin ifadesini yıkmak |
| ⑤ (isteğe bağlı) | pozitif siRNA | Deneysel sistem ve operasyonel sorunları gidermek için kullanılır |
| ⑥ (isteğe bağlı) | Floresan kontrol siRNA | Hücre transfeksiyonunun etkinliği mikroskopla gözlemlenebilir |
2.2 Primer tasarım ilkeleri
| Güçlendirilmiş parça boyutu | Tercihen 100-150bp'de |
| Astar Uzunluğu | 18-25bp |
| GC içeriği | %30 - %70, tercihen %45 - %55 |
| değer | 58-60 ℃ |
| Sekans | Sürekli T/C'den kaçının;A/G sürekli |
| 3 bitiş sırası | GC zengini veya AT zengininden kaçının;terminal tabanı tercihen G veya C'dir;T'den kaçınmak en iyisidir |
| tamamlayıcılık | Primer içinde veya iki primer arasında 3'ten fazla bazın tamamlayıcı sekanslarından kaçının |
| özgüllük | Primer özgüllüğünü doğrulamak için patlama aramasını kullanın |
①SiRNA türe özgüdür ve farklı türlerin dizilimleri farklı olacaktır.
②SiRNA, oda sıcaklığında 2-4 hafta stabil bir şekilde saklanabilen dondurularak kurutulmuş toz halinde paketlenir.
2.3 Önceden hazırlanması gereken araçlar veya reaktifler
| Astar (dahili referans) | İleri ve geri iki dahil |
| Primerler (hedef gen) | İleri ve geri iki dahil |
| Hedef Si RNA (3 şerit) | Genel olarak, şirket 3 şeridi sentezleyecek ve ardından RT-PCR ile üç şeritten birini seçecektir. |
| Transfeksiyon Kiti | Lipo2000 vb. |
| RNA Hızlı Ekstraksiyon Kiti | Transfeksiyondan sonra RNA ekstraksiyonu için |
| Hızlı Ters Transkripsiyon Kiti | cDNA sentezi için |
| PCR Amplifikasyon Kiti | 2×Süper SYBR Yeşil qPCR Ana Karışımı |
2.4 Belirli deneysel adımlarda dikkat edilmesi gereken hususlarla ilgili olarak:
①siRNA transfeksiyon işlemi
1. Kaplama için 24 kuyulu plaka, 12 kuyulu plaka veya 6 kuyulu plaka seçebilirsiniz (24 kuyulu bir plakanın her kuyusunda önerilen ortalama RNA konsantrasyonu yaklaşık 100-300 ng/uL'dir) ve hücrelerin optimal transfeksiyon yoğunluğu %60-%80'e kadardır
2. Transfeksiyon adımları ve özel gereksinimler kesinlikle talimatlara uygundur.
3. Transfeksiyondan sonra, mRNA saptaması (RT-PCR) için örnekler 24-72 saat içinde veya 48-96 saat içinde protein saptaması (WB) için toplanabilir.
② RNA çıkarma işlemi
1. Eksojen enzimler tarafından kontaminasyonu önleyin.Esas olarak kesinlikle maske ve eldiven takmayı içerir;steril pipet uçları ve EP tüpleri kullanarak;deneyde kullanılan su RNase Free olmalıdır.
2. Saflığı ve verimi gerçekten artıracak olan hızlı ekstraksiyon kitinde önerildiği gibi iki kez yapılması önerilir.
3. Atık sıvı RNA kolonuna temas etmemelidir.
③ RNA ölçümü
RNA ekstrakte edildikten sonra doğrudan Nanodrop ile ölçülebilir ve minimum okuma 10ng/ul kadar düşük olabilir.
④Ters transkripsiyon işlemi
1. RT-qPCR'nin yüksek duyarlılığı nedeniyle, sonraki Ct'nin çok farklı olmasını veya SD'nin istatistiksel analiz için çok büyük olmasını önlemek için her örnek için en az 3 paralel kuyu yapılmalıdır.
2. Master mix'i tekrar tekrar dondurup çözmeyin.
3. Her tüp/delik yeni bir uç ile değiştirilmelidir!Numune eklemek için sürekli olarak aynı pipet ucunu kullanmayın!
4. Numune eklendikten sonra 96 oyuklu plakaya yapıştırılan filmin bir plaka ile düzleştirilmesi gerekir.Makineye koymadan önce santrifüj yapmak en iyisidir, böylece tüp duvarındaki sıvı aşağı akabilir ve hava kabarcıklarını giderebilir.
⑤Ortak eğri analizi
| Logaritmik büyüme dönemi yok | Muhtemelen yüksek şablon konsantrasyonu |
| BT değeri yok | Floresan sinyalleri algılamak için yanlış adımlar; primerlerin veya probların bozulması – bütünlüğü PAGE elektroforezi ile tespit edilebilir; yetersiz miktarda şablon; şablonların bozunması – numune hazırlama sırasında safsızlıkların ve tekrarlanan donma ve çözülmenin önlenmesi; |
| Ct>38 | Düşük amplifikasyon verimliliği;PCR ürünü çok uzun;çeşitli reaksiyon bileşenleri bozulur |
| Lineer amplifikasyon eğrisi | Problar, tekrarlanan donma-çözülme döngüleri veya uzun süre ışığa maruz kalma nedeniyle kısmen bozulabilir. |
| Yinelenen deliklerdeki fark özellikle büyüktür | Reaksiyon solüsyonu tamamen erimemiş veya reaksiyon solüsyonu karıştırılmamış;PCR aletinin termal banyosu flüoresan maddelerle kirlenmiştir |
2.5 Veri analizi hakkında
qPCR'nin veri analizi, göreli niceleme ve mutlak niceleme olarak ikiye ayrılabilir.Örneğin, tedavi grubundaki hücreler kontrol grubundaki hücrelerle karşılaştırıldığında,
X geninin mRNA'sının kaç kez değiştiği, bu göreceli nicelemedir;belirli sayıda hücrede, X geninin mRNA'sı
Kaç tane kopya var, bu mutlak nicelemedir.Genellikle laboratuvarda en çok kullandığımız göreceli kantitatif yöntemdir.Genellikle,2-ΔΔct yöntemideneylerde en çok kullanıldığı için burada sadece bu yöntem ayrıntılı olarak tanıtılacaktır.
2-ΔΔct yöntemi: Elde edilen sonuç, deney grubundaki hedef genin ekspresyonunun kontrol grubundaki hedef gene göre farkıdır.Hem hedef genin hem de dahili referans genin amplifikasyon verimlerinin %100'e yakın olması ve bağıl sapmanın %5'i geçmemesi gerekir.
Hesaplama yöntemi aşağıdaki gibidir:
Δct kontrol grubu = kontrol grubundaki hedef genin ct değeri – kontrol grubundaki dahili referans genin ct değeri
Δct deney grubu = deney grubundaki hedef genin ct değeri – deney grubundaki dahili referans genin ct değeri
ΔΔct=Δct deney grubu-Δct kontrol grubu
Son olarak, ifade seviyesindeki farkın katını hesaplayın:
Change Fold=2-ΔΔct (excel işlevine karşılık gelen GÜÇ'tür)
İlgili ürünler:
Gönderim zamanı: 20 Mayıs-2023